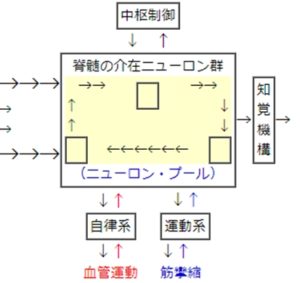
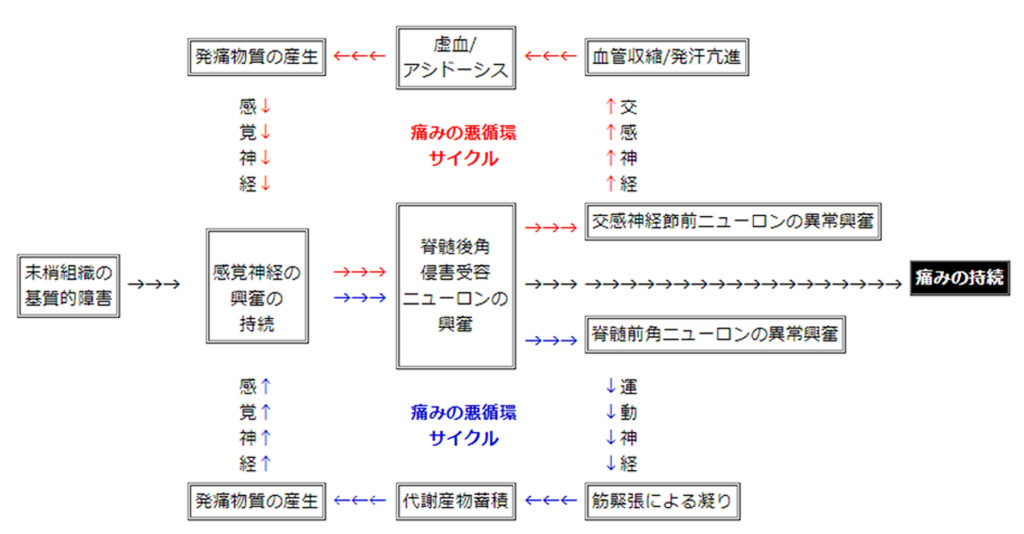
ゲート・コントロールセオリー:Patrick D. WallとRonald Melzackが1965年に提唱したゲート・コントロールセオリー (Science: 150, 971-979, 1965)
1)ゲート・コントロールセオリーは単に触刺激によって痛みが押さえられるメカニズムを説明したものではない。「脊髄後角に、痛み信号の流入をコントロールするゲートの機能がある。」
2)シンプルなシェーマで描かれたゲートは、脊髄後角には残念ながら存在しない。
3)ゲート・コントロールセオリーは痛みの感覚的側面だけで痛みを説明したものではなく、情動・認知的側面から感覚的側面へのフィードバックという新しい概念を取り入れたことに大きな意義があった。
4)のセオリーには多くの誤りがあったが、その後の脊髄後角の侵害受容ニューロンの研究や痛みの鎮痛治療法(TENSやDCS)の発展に大きく貢献した。
○ゲート・コントロールに至った研究
William Noordenbos(1910~1992、アムステルダムの脳外科医)は1959年に感覚と病理実験を結合して、帯状疱疹後神経痛を理解する説を提唱した。患部の中心部では、触覚が消失しているにもかかわらず、痛覚が増強していた。肋間神経をバイオプシーすると、太い有髄線維が選択的に減少し、細い線維の数が相対的に増加していることを見出した。太い有髄神経の減少することによって、C線維を介して起こされる痛みに対する中枢性の抑制効果が減少するために痛みが増強するという説を提唱した。さらに、脊髄後角の膠様質が時間的、空間的収束に大きな役割を果たすと示唆した。マルチシナプスによる修飾を想定したが、実験的な裏付けを見つけることはできなかった。しかし、脊髄後角へのC線維の入力が制御されない効果というNoordenbosのmultisynaptic modification system は、ゲート・コントロール説に大きな影響を及ぼした。1/*
Lorne MendellとPatrick D. Wallは膠様質をシナプス前抑制性介在ニューロンと考えていた。←参考1/2
末梢神経に含まれる太い線維を電気刺激すると陰性後根電位が発生する。太い線維の興奮伝導を遮断しておいてから、C線維に電気刺激を加えると陽性後根電位が発生すると報告した。陰性後根電位は、求心性線維終末部の脱分極によるもので、求心性線維のシナプス伝達を抑制する。陽性後根電位は求心性線維終末部の過分極によるものでシナプス伝達を促進する。
○1965年のゲート・コントロール説
1)末梢神経により運ばれるインパルス
→脊髄の後索核
→脊髄後角膠様質ニューロン(SG)
→脊髄後角の第1次中心伝達細胞(T細胞)
2)脊髄に入る求心性線維
→太いL線維(AδおよびAβ線維)
→細いS線維(Aδ線維とC線維)
3)神経線維の活動
細い線維は刺激がないときも自発性のインパルスを送る。
4)L線維から、SGとT細胞の両方を興奮性入力がある。
5)S線維入力はSGを抑制し、T細胞を興奮させる。
6)SGは、L線維とS線維の終末にシナプス前抑制をかけている。
7)末梢からのインパルスがT細胞に到達するためには、SGが作るゲートを開かねばならない。
8)侵害防御反応や痛み情報が脳に伝わるためには、T細胞のインパルスの興奮作用の時間的・空間的加重による総和が一定値を越えて、活動系が開始する必要がある。
末梢刺激がないときには、S線維の自発放電によって、ゲートは開いている。
末梢に弱い刺激が加わると、L線維からの入力によりSGが興奮すると、ゲートがすぐ閉ざされ、後続インパルスのT細胞への伝達が遮断される。
刺激がさらに強まると、S線維が興奮に加わる。強い刺激を長く与えると、L線維は順応するが、S線維は興奮を持続する。その結果ゲートが開かれて、T細胞にインパルスが到達する。Tの興奮が一定値を越え活動系が作動しはじめて、痛みが起こり、侵害刺激に対する反応も現れる。
ここで皮膚に弱い刺激を加えるとゲートが再閉鎖されて、痛みが弱まる。この関門には上位中枢からの制御も加わる。脊髄の後索を上行したインパルスが大脳皮質に中継され、錐体路をへて脊髄に戻ってくるフィードバック回路もその一つで、それはゲートを閉鎖する。
■ゲートコントロールセオリーの神経メカニズムについてのサマリー
1)ゲートコントロールセオリーの主役は、SG: substantia gelatinosa(膠様質)のニューロンである。
2)SGは、痛みの信号を伝するT細胞に対するゲートを閉じる働きをしている。
3)侵害性の高閾値感覚を伝える細い神経線維は、SGを抑制するので、痛みの信号伝達のゲートが開き、痛みを感じる。
4)触、圧、振動などの低閾値感覚を伝える太い神経線維は、SGを活性化させるので、痛みの信号の通路のゲートを閉ざす。
5)経皮的電気刺激(TENS)もこの機序を応用したもので、Aβ線維を刺激することで、痛覚を分節性に制御する。
6)このような、低閾値感覚が痛覚伝導路に影響を及ぼす機序は、脊髄だけではなく、視床や大脳皮質のレベルにおいてもみられると考えられる。
○ゲート・コントロール説とあわない事実
1)C線維に電気刺激を加えると陰性後根電位が発生する。
2)細い線維は刺激がないときも自発性のインパルスを送るか?
3)太い線維は膠様質に興奮性入力を送るか?
4)細い線維は膠様質に抑制性入力を送るか?
5)細い線維による興奮がSG細胞の過分極を起こし、シナプス前抑制を脱抑制するか?
6)帯状疱疹後神経痛では、太い線維が特異的に減少するか?
7)フリードライヒ失調症では太い線維が選択的に傷害される(?)が、痛みが生じない。
8)脊髄侵害受容ニューロンに対する抑制系は、ゲート・コントロールだけではない。
○修正されたゲート・コントロール説
組織のその傷害の情報は、細い線維(Aδ線維とC線維)によって中枢に伝えられるが、これには2種類あって、傷害のみに反応するものと、より低い刺激閾値を持つが、刺激の強さが侵害刺激のレベルに達すると興奮頻度を増すものとがある。
脊髄後角や三叉神経脊髄路核には傷害信号を運ぶ末梢神経のインパルスによって興奮するニューロンがあり、その興奮は非侵害性信号を運ぶ末梢神経のインパルスによって変えられる。
傷害信号を中継するニューロンの興奮は、脳から下行する制御系によって変えられる。
↓
脳は、侵害受容性信号、非侵害受容性信号および下行制御の影響下にあるゲートコントロール系を経由したメッセージを受け入れる。
細い侵害受容線維の興奮が常に同じ感覚を引き起こすとは限らず、侵害受容に直接関与しない神経線維の興奮や、脳の状態によって強調が加えられる。